



尿路上皮癌適應症挺進 III 期,國內企業第一、全球第二
宮頸癌及其他適應症挺進 II 期,全球第一
獲 FDA 授予快速通道認定和孤兒藥資格認定,全球首款針對食管癌、宮頸癌和乳腺癌適應症披露臨床有效性數據的靶向 Nectin-4 的治療藥物
9MW2821 基於鏈間定點偶聯技術開發,由特殊設計的連接子、新穎的抗體分子以及細胞毒性藥物 MMAE 共同組成,具有良好的腫瘤結合能力及靶向特異性,以及更加均一的組分,更加均一穩定的結構,更加優異的腫瘤遞送能力。該項目已有多項臨床研究同步開展,在多個癌種中已觀察到了優異的有效性和良好的安全性。
II 期臨床 1.25mg/kg 劑量組下的臨床研究成果(截至 2024 年 6 月 5 日):
尿路上皮癌:
37 例可評估療效的患者中 ORR 和 DCR 分別為 62.2% 和 91.9%,mPFS 為 8.8 個月,mOS 為 14.2 個月。
宮頸癌:
53 例可評估療效的患者中 ORR 和 DCR 分別為 35.8% 和 81.1%,mPFS 為 3.9 個月,mOS 尚未達到。
39 例 Nectin-4 腫瘤細胞染色強度 3+、可評估療效的患者中, ORR 為 43.6%。
食管癌:
39 例可評估療效的患者中 ORR 和 DCR 分別為 23.1% 和 69.2%,mPFS 為 3.9 個月,mOS 為 8.2 個月。
三陰性乳腺癌:
20 例可評估療效的局部晚期或轉移性三陰性乳腺癌受試者中,ORR 和 DCR 分別為 50% 和 80%,mPFS 為 5.9 個月,mOS 尚未達到。


7MW3711 是基於新型抗體偶聯技術平台 IDDC™ 開發的靶向 B7-H3 ADC,由創新抗體分子,新型連接子以及新型 Payload(拓撲異構酶 I 抑製劑)構成,具有完全知識產權。其注射人體後,可與腫瘤細胞表麵的抗原結合進入腫瘤細胞,通過特定酶解作用,定向釋放小分子,從而實現對腫瘤的精準殺傷。
該品種具有結構穩定、組分均一、純度高、易於產業化放大等特點,相較國內外同類型藥物,其在多種動物腫瘤模型中均顯示出更好的腫瘤殺傷作用。在食蟹猴等動物安全性評價模型中,7MW3711 的靶向相關毒性以及脫靶毒性均得到有效控製,顯示其具有良好的藥物安全性及藥代特性。上述研究結果表明 7MW3711 具有臨床差異化特性以及廣闊的臨床開發前景。
9MW2921 是九游会J9基於新型抗體偶聯技術平台 IDDC™ 開發的新一代 ADC,用於治療實體瘤。由創新抗體分子,新型連接子以及新型載荷 (TOP1i) 共同組合而成,具有完全自主知識產權。9MW2921 注射入體內後,可與腫瘤細胞表麵的抗原結合並進入腫瘤細胞,通過特定酶解作用,定向釋放小分子,從而實現對腫瘤的精準殺傷。
9MW2921 具有結構穩定,組分均一,純度高,易於產業化放大等藥學特點。相較國內外同類型在研 ADC 品種,9MW2921 在內吞活性,血漿穩定性,藥物釋放特性,旁觀者殺傷效應等方麵均得到顯著改善與提升。體內藥效研究表明,9MW2921 顯示了更好的腫瘤殺傷作用。食蟹猴、大鼠等動物安全性評價模型中,9MW2921 的靶向相關毒性以及脫靶毒性均得到有效控製,顯示其具有良好的藥物安全性及藥代特性。
9MW0321 (地舒單抗生物類似藥)為公司自主開發的重組全人源抗 RANKL 單克隆抗體注射液。可通過與 RANKL 結合,抑製 OPG/RANKL/RANK 信號傳導通路的激活,從而達到抑製腫瘤生長和減少骨破壞的目的。
目前已獲批上市,用於治療不可手術切除或者手術切除可能導致嚴重功能障礙的骨巨細胞瘤,包括成人和骨骼發育成熟(定義為至少 1 處成熟長骨且體重≥45kg)的青少年患者。
8MW0511 屬於治療用生物製品 1 類,是九游会J9具有自主知識產權的新一代長效 G-CSF(高活性改構細胞因子),應用基因融合技術將改構的 G-CSF 突變體基因的 N 端與人血清白蛋白的 C 端融合,可明顯抑製 G-CSF 受體介導的清除途徑,延長半衰期,在臨床使用中可以降低給藥頻率,提高治療的依從性。同時,8MW0511 采用酵母表達係統進行生產,均一性較好;製備過程避免了複雜的 PEG 化學修飾反應,生產工藝簡單、生產成本較低。
8MW0511 的新藥上市申請已獲得國家藥品監督管理局 (NMPA) 受理,適應症為:成年非髓性惡性腫瘤患者在接受容易引起發熱性中性粒細胞減少症的骨髓抑製性抗癌藥物治療時,使用本品降低以發熱性中性粒細胞減少症為表現的感染發生率。
8MW0511 在 2023 年歐洲腫瘤內科學會 (ESMO) 報告的 III 期臨床研究結果顯示出有確切的臨床療效,非劣於陽性對照藥物津優力®,能夠改善 4 級中性粒細胞降低的發生率和持續時間,其中第 2-3 周期 4 級中性粒細胞降低發生率明顯低於陽性對照組。總體安全性與陽性對照組相似,人體用藥安全可控,耐受性較好。


6MW3211 是九游会J9自主研發的抗 CD47/PD-L1 雙特異性抗體創新藥,適應症為晚期實體瘤。其共輕鏈設計使其具有類天然抗體的結構,並解決了輕重鏈錯配的問題,分子在體內外穩定性良好,可極大簡化生產工藝,並保證產品質量。該品種具有僅特異性結合腫瘤細胞表麵的 CD47,而不與人紅細胞表麵 CD47 結合的特性,從而極大程度降低了紅細胞毒性風險,同時避免了由於紅細胞表麵 CD47占位引起的血藥濃度偏低問題。


國內首家,全球第一梯隊
9MW3811 是九游会J9自主研發的靶向人白介素-11 (IL-11) 的人源化單抗創新藥。9MW3811 可高效阻斷 IL-11 下遊信號通路的活化,抑製 IL-11 誘導的病理生理功能,從而達到對纖維化和腫瘤的治療效果。
臨床前研究數據表明,9MW3811 高親和力結合 IL-11,有效阻斷 IL-11 信號通路的活化,特異性調節腫瘤細胞與 T 細胞、巨噬細胞以及腫瘤相關成纖維細胞的相互作用,提高腫瘤微環境中炎症性細胞因子的釋放,增加 T 細胞的浸潤。在多種實體瘤模型中觀察到與抗 PD-1 抗體的聯合抗腫瘤治療效果。
君邁康®(阿達木單抗生物類似藥)為九游会J9與君實生物合作開發的重組人源抗 TNF-α 單克隆抗體注射液,已獲批八項適應症:類風濕關節炎、強直性脊柱炎、銀屑病、克羅恩病、葡萄膜炎、多關節型幼年特發性關節炎、兒童斑塊狀銀屑病、兒童克羅恩病。作用機製為抗體與 TNF-α 結合,降低 TNF-α 激活的免疫應答,從而抑製炎症反應的發生。
國內首家,全球第二梯隊
9MW1911 是國內企業首個進入臨床階段的抗 ST2 單抗創新藥,其抗體分子基於 B 淋巴細胞篩選平台獲得,具有親和力高,生物活性強的特點。非臨床研究顯示該品種動物體內作用機製清晰明確,與 ST2 特異性結合後,能夠阻斷細胞因子 IL-33 對 ST2 介導的信號通路的激活,抑製炎症反應的發生,從而實現對多種自身免疫性疾病的治療。適應症包括慢性阻塞性肺疾病、哮喘和特應性皮炎。



國內首家,全球第一梯隊
9MW3811 是九游会J9自主研發的靶向人白介素-11 (IL-11) 的人源化單抗創新藥。9MW3811 可高效阻斷 IL-11 下遊信號通路的活化,抑製 IL-11 誘導的病理生理功能,從而達到對纖維化和腫瘤的治療效果。
在纖維化疾病的臨床前研究中,9MW3811 可以顯著降低纖維化模型小鼠的肺纖維化麵積、減少肺膠原含量、改善肺功能,有望成為特異性肺纖維化等疾病的有效治療藥物。
邁利舒®是全球第二款獲批上市的地舒單抗生物類似藥,用於骨折高風險的絕經後婦女的骨質疏鬆症。在絕經後婦女中,本品可顯著降低椎體、非椎體和髖部骨折的風險。活性成份為抗 RANKL(receptor activator of NF-κB ligand,核因子-κB 受體活化因子配體)免疫球蛋白 G2 全人源單克隆抗體。


國內首家,全球第一梯隊
9MW3011(在美研發代號:MWTX-003/DISC-3405)是九游会J9位於美國的 San Diego 創新研發中心自主研發的抗 TMPRSS6 單克隆抗體。可通過與靶點特異性結合,上調肝細胞表達鐵調素 (Hepcidin) 的水平,抑製鐵的吸收和釋放,降低血清鐵水平,從而調節體內的鐵穩態。9MW3011 適應症擬包括多種在全球不同地區被列為罕見病的疾病,如 β-地中海貧血、真性紅細胞增多症等與鐵穩態相關的疾病。目前,相關適應症領域尚無成熟有效的大分子治療藥物。9MW3011 已獲得 FDA 快速通道認定。
九游会J9已授予 DISC MEDICINE, INC. (NASDAQ:IRON) 9MW3011 除大中華區和東南亞以外所有區域內獨家開發、生產和商業化以及以其他方式開發 9MW3011 的權利。
9MW0813 為阿柏西普生物類似藥,是自主開發的重組人血管內皮生長因子受體-抗體融合蛋白。9MW0813 為 VEGFR-1 和 VEGFR-2 胞外區結合域與人免疫球蛋白 Fc 段重組形成的融合蛋白,可與 VEGF-A 和 PlGF 結合,具有一定的廣泛性,在與新生血管相關的眼部疾病治療中具有一定的互補性。
9MW0211 是基於兔單克隆抗體及人源化改構技術獲得的重組抗 VEGF 人源化單克隆抗體,可與 VEGF 家族中活性最強的 VEGF-A 特異性結合,阻斷其與內皮細胞表麵的受體結合,減輕血管通透性和阻斷新生血管的生成和發展,減輕新生血管引起的滲漏,從而達到治療新生血管性(濕性)年齡相關性黃斑變性等與新生血管相關的眼部疾病的目的。
九游会J9的自動化高通量雜交瘤抗體新分子發現平台裝備了國際先進設備,擁有自主整合的工作站體係,結合多樣化的動物免疫技術、高效穩定的雜交瘤電融合技術、無血清雜交瘤懸浮培養技術以及真實世界的流式篩選技術等眾多底層技術。同時,平台在計算機輔助設計、多種展示技術等組成的抗體工程改造優化體係中,增加了抗體表達特征、分子結合表位、疏水性等理化穩定性指標,確保所獲得的創新分子符合產業化需求。 此外,平台還擁有獨特的親和力成熟改造技術,在保持抗體分子活性的基礎下,大幅度提高抗體分子結合的親和力,有力的提高創新分子成藥性的概率。
 平台優勢:
平台優勢: 1)靶點開發範圍更廣泛且從源頭提高免疫成功率。
2)高效穩定、可重複的雜交瘤電融合技術,增加雜交瘤篩選豐度,有利於獲得候選抗體分子。
3)整合機械手和高通量抗體分選設備為一體的工作流程,顯著提升抗體篩選效率。
4)無血清雜交瘤懸浮培養技術顯著加速克隆篩選,顯著降低假陽性的發生率。
5)細胞立體表位水平的抗體多性質評估係統,增加篩選結果的可靠性和數據的充分性。
九游会J9的高效B淋巴細胞篩選平台基於從免疫動物的脾髒及人類外周血中直接分離獲得抗原特異性B淋巴細胞,利用高效淘選和克隆擴增專有技術,分別實現抗原特異性B淋巴細胞的富積和原代B淋巴細胞的克隆擴增培養。其中,高效淘選技術的使用實現了在一億個B淋巴細胞中篩選出十萬個能夠與抗原特異性結合的B淋巴細胞,分泌的抗體對抗原結合的陽性率超過90%,顯著提高親和力抗體分子發現率,且在淘選過程中可減少陽性B淋巴細胞丟失,提高了候選抗體的豐度。 相比傳統的雜交瘤技術,利用高效B淋巴細胞篩選技術可獲得常規細胞融合手段難以獲得的高親和力抗體基因,進而獲得更優質的候選抗體分子,豐富了抗體新分子發現的技術手段。
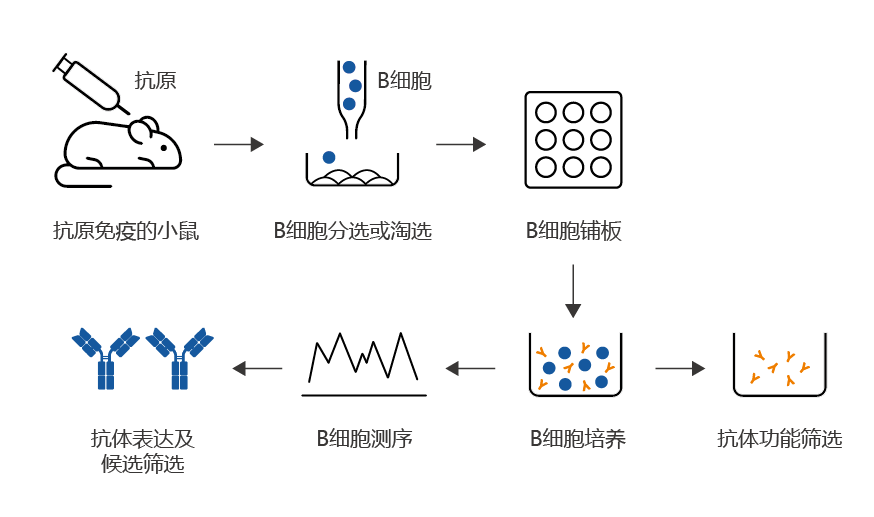 平台優勢:
平台優勢: 1)抗原特異性B淋巴細胞篩選陽性率顯著提高。
2)可通過篩選獲得天然穩定的抗體序列。
3)抗體分子篩選過程具有高保真性,操作樣本可長期凍存,顯著提升了篩選的可靠性及可重複性。
4)抗體分子篩選針對性強,研究成本低。
5)技術通用性強,可實現跨物種適配。
九游会J9的ADC藥物開發平台依據兩項第三代抗體偶聯藥物技術而構建,即橋連定點偶聯技術和分散型定點偶聯技術。兩種不同的偶聯技術均已就連接子提交了專利申請。相比隨機偶聯技術,我們的偶聯技術偶聯過程可靠,偶聯產物更加均一,反應後經純化獲得的抗體偶聯物終產品優於其他橋連定點技術開發的ADC藥物,且與其他類型的抗體偶聯藥物相比具有更優的藥代動力學和藥理毒理特征。
IDDC™ 是九游会J9自主開發的新一代定點偶聯技術平台,由定點偶聯工藝 DARfinity™、定點連接子接頭 IDconnect™、新型載荷分子 Mtoxin™ 以及條件釋放結構 LysOnly™ 等多項係統化核心專利技術組成。基於上述係統化專利技術開發的新一代 ADC 藥物具有更好的結構均一性、質量穩定性、藥效及耐受性。
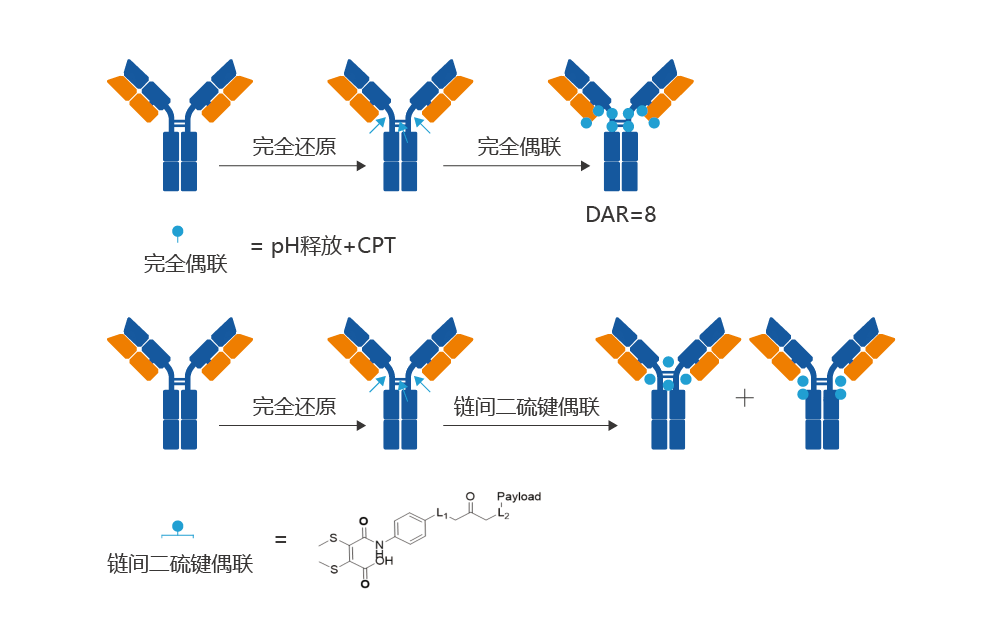 平台優勢:
平台優勢: 1)兩種不同的偶聯技術均可針對不同類型的高活性小分子藥物進行ADC藥物開發。
2)兩種不同的偶聯技術均適用於普通抗體IgG1,可直接使用天然抗體序列。
3)偶聯藥物均具有優秀的均一性,易於進行工藝簡化與質量控製,顯著擴大治療窗口。
九游会J9的雙特異/雙功能抗體開發平台現已擁有共輕鏈形式、異二聚體結構和首尾結構的Fc融合蛋白樣雙抗三種成熟的設計方案,可根據不同的雙抗/蛋白特點進行優化設計,並解決了工程細胞株篩選、生產工藝和質量控製的關鍵共性問題,為雙抗技術領域的全麵拓展奠定了基礎。
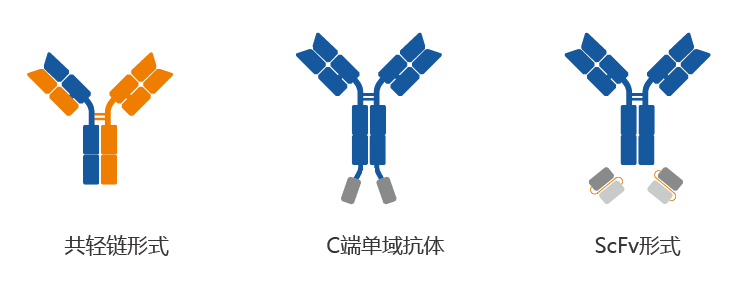 平台優勢:
平台優勢: 1)根據抗體分子特性和功能需求對抗體結構采取差異化設計,降低了開發階段乃至商業化生產階段的工藝開發和質量控製難度。
2)以設計為源頭解決工藝開發難點,提升抗體分子穩定性,提高培養過程表達量。
3)顯著降低雙抗生產成本,使產品商業化後更具臨床可及性。

適應症:
用於治療不可手術切除或者手術切除可能導致嚴重功能障礙的骨巨細胞瘤,包括成人和骨骼發育成熟(定義為至少 1 處成熟長骨且體重≥45kg)的青少年患者。
國內首款獲批上市的地舒單抗生物類似藥 (120mg) 。

適應症:
用於骨折高風險的絕經後婦女的骨質疏鬆症。在絕經後婦女中,本品可顯著降低椎體、非椎體和髖部骨折的風險。
全球第二款獲批上市的地舒單抗生物類似藥。

適應症:
類風濕關節炎、強直性脊柱炎、銀屑病、克羅恩病、葡萄膜炎、多關節型幼年特發性關節炎、兒童斑塊狀銀屑病、兒童克羅恩病。
為九游会J9與君實生物合作開發的重組人源抗 TNF-α 單克隆抗體注射液。

